No manejo da esclerose múltipla (EM), duas estratégias terapêuticas foram propostas. Alguns defendem uma abordagem de escalonamento, postulando que a prioridade deve ser a segurança. Entretanto, caso durante o monitoramento, o paciente apresente doença mais agressiva, evidenciada por surtos clínicos, alterações ao exame de ressonância magnética nuclear (RMN) ou progressão da incapacidade, deve-se considerar fortemente a troca para uma terapia de maior eficácia.1
Um segundo modelo é a “terapia de indução” ou uma abordagem precoce com terapia de alta eficácia (TAE). Os proponentes da TAE desde o início do tratamento da EM argumentam que a possibilidade atual de se prever a evolução da doença em longo prazo é limitada, assim como a possibilidade de detecção de lesões continuadas no sistema nervoso pela EM. Além disso, os defensores da TAE precoce consideram o perfil de risco de algumas opções atuais equiparável ao de terapias menos eficazes.1 (Figura 1)
Figura 1. Terapia de escalonamento e terapia de alta eficácia precoce no manejo da EM
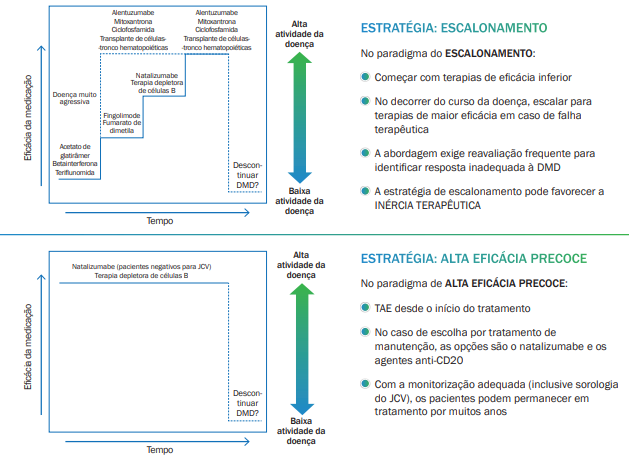
Adaptada de: Gross RH, Corboy JR. Continuum (Minneap Minn). 2019 Jun;25(3):715-735.2
Evidências em favor das terapias de alta eficácia desde o início do tratamento
Com os avanços no conhecimento da fisiopatologia da EM ocorridos nos últimos anos, o uso precoce das TAE vem sendo proposto como estratégia preferencial para obter os melhores resultados clínicos no longo prazo em pacientes com EM.1 Em um artigo publicado em 2019, James Stankiewicz e Howard Weiner, da Escola Médica de Harvard, defendem uma ampla utilização das terapias de alta eficácia precocemente no curso da EM, em contraposição à terapia de escalonamento. Os principais argumentos apresentados no artigo estão resumidos no quadro 1.1
Quadro 1. Argumentos em favor do uso de terapias de alta eficácia desde o início do tratamento da EM

Estudos de patologia e de ressonância magnética nuclear (RMN) indicam que a EM é uma condição neurológica cronicamente progressiva, e não uma doença episódica, e que comumente a extensão dos danos cerebrais e medulares dos pacientes ao longo do tempo é subestimada. Além disso, atualmente é difícil prever, na apresentação inicial da doença, quais pacientes terão uma evolução mais benigna no longo prazo, mesmo com um cuidadoso monitoramento prospectivo da atividade da doença. Com os avanços recentes no cenário do tratamento da EM, o risco de danos ao sistema nervoso em um paciente com EM supera amplamente eventuais preocupações com efeitos colaterais graves das terapias de alta eficácia. Assim, os autores concluem que os neurologistas e os gestores das políticas de saúde proporcionarão maior benefício aos pacientes com EM adotando estratégias baseadas no uso precoce das terapias de alta eficácia.1 A figura 1 resume, em linhas gerais, as principais características das estratégias de escalonamento e do uso precoce de terapia de alta eficácia para pacientes com EM.1,2
Melhores desfechos clínicos com as terapias de alta eficácia
Um estudo com dados do registro MSBase e do programa de observação dos pacientes tratados com natalizumabe (TOP, do original TYSABRI Observational Program) comparou pacientes que passaram a receber natalizumabe com pacientes que alternaram entre acetato de glatirâmer (AG) ou uma betainterferona (IFN-β) após apresentarem surto da doença durante o tratamento com IFN-β ou AG. Os grupos de tratamento foram balanceados por meio de um pareamento baseado em escores de propensão no início do tratamento, na população global (n=869/grupo) e em subgrupos baseados no tratamento prévio (n=578/grupo somente com IFN-β, n=165/grupo somente com AG e n=176/grupo com ambos). Os principais resultados do estudo estão resumidos no quadro 2.3
Quadro 2. Desfechos clínicos observados com a troca do tratamento para natulizumabe vs. AG ou IFN-β em pacientes com EM
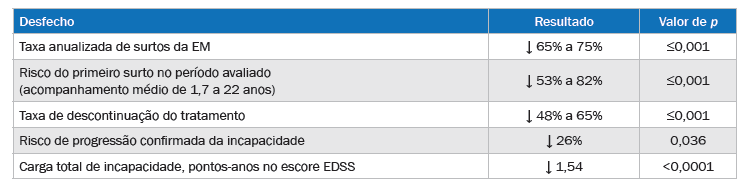
Em outro estudo retrospectivo envolvendo uma coorte de 193 pacientes com EM recorrente-remitente (EMRR) tratados com natalizumabe no Hospital Universitário de Praga, na República Checa, foram avaliados parâmetros da RMN e também o desfecho chamado NEDA-3. O termo NEDA significa “sem evidências de atividade da doença” (do inglês no evidence of disease activity). Considera-se que o desfecho NEDA-3 foi atingido se o paciente não apresentar surtos da doença nem progressão da incapacidade confirmada após seis meses e não houver lesões novas ou aumentadas na sequência FLAIR da RMN. A proporção de pacientes sem lesões novas ou aumentadas na sequência FLAIR da RMN após 2 a 5 anos de tratamento com natalizumabe (desfecho primário do estudo) foi ≥98,0%, e a proporção de pacientes sem novas lesões em T1 da RNM, no mesmo período, foi ≥98,8%. No primeiro ano de tratamento com natalizumabe, 52,2% atingiram o desfecho NEDA-3, proporção que aumentou para ≥69,2% em 2 a 5 anos.4
O estudo prospectivo e randomizado de fase 4 REVEAL comparou a eficácia de natalizumabe e fingolimode em 108 pacientes com EMRR de nove países. A figura 2 ilustra o número cumulativo médio de novas lesões realçadas por gadolínio nas imagens de RMN ponderadas em T1 ao longo de 24 semanas, nos pacientes tratados com fingolimode e natalizumabe. Além disso, a probabilidade cumulativa de um surto ao longo do acompanhamento foi de 1,9% com natalizumabe e 22,3% com fingolimode (razão de risco [HR]: 0,08; intervalo de confiança [IC] de 95%: 0,01 a 0,64; p=0,017, figura 3). Os resultados sugerem maior benefício do natalizumabe, em comparação com o fingolimode, na redução das taxas de surto da doença e no acúmulo de lesões realçadas em gadolínio na RMN em pacientes com EMRR ativa. O início da eficácia ocorreu mais rapidamente com natalizumabe, comparado ao fingolimode, o que pode ser um fator importante na escolha do tratamento em pacientes com doença ativa, que necessitam de um controle rápido e eficaz da EM.4
Figura 2. Número cumulativo médio de novas lesões Gd+ em imagens de RMN ponderadas em T1 ao longo de 24 semanas do estudo REVEAL
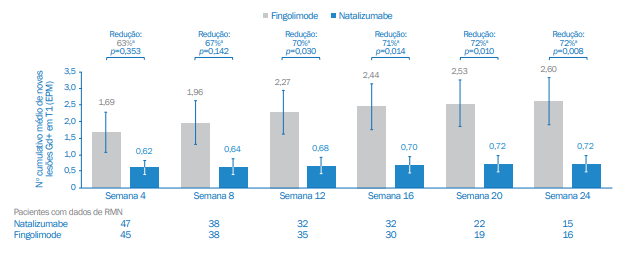
Figura 3. Curvas de sobrevida de Kaplan-Meier do tempo até um surto da EM ao longo de 52 semanas
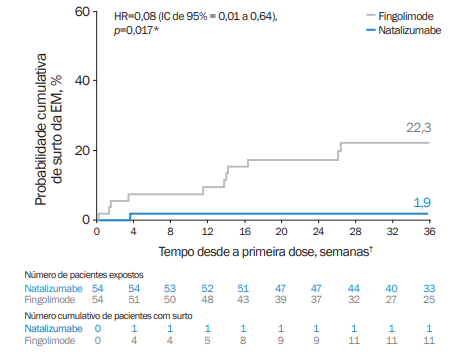
EM: esclerose múltipla; EDSS: Escala Expandida do Estado de Incapacidade (Expanded Disability Status Scale); HR: razão de risco. Adaptada de: Butzkueven H, et al. BMJ Open. 2020 Oct 20;10(10):e038861.5
Os riscos da inércia terapêutica no manejo da EM
Como alerta o já citado artigo de Stankiewicz e Weiner, a inércia terapêutica pode contribuir para a perda de tecido cerebral e, consequentemente, da reserva neurológica em pacientes com EM.1 Ao analisar os desfechos de longo prazo em uma coorte populacional de 592 pacientes com EM em função da estratégia terapêutica inicial, Harding et al. observaram um período mediano de 2,4 anos (IC de 95%: 2,1 a 3,5) para o escalonamento das terapias modificadoras da doença, entre os pacientes que iniciaram com terapia de eficácia moderada. Além disso, os desfechos no longo prazo foram mais favoráveis à terapia inicial de alta eficácia, comparada às opções de moderada eficácia. Os autores ponderam que as estratégias atuais de vigilância e os protocolos de escalonamento podem ser pouco responsivos à progressão das lesões e da incapacidade em pacientes com EM.6
Os fatores indicativos de conversão para a fase progressiva da EM incluem o tempo para acumular três pontos no escore EDSS, altas taxas de surtos nos primeiros dois anos de doença e intervalos curtos entre os surtos. Há um subgrupo de pacientes com EMRR que manifestam doença mais agressiva, com rápido acúmulo de incapacidades físicas e cognitivas, chamada EM altamente ativa. Para esses pacientes, a janela terapêutica fecha-se rapidamente.7
Como o alvo principal das DMDs é o processo inflamatório no sistema nervoso central (SNC), as terapias são mais efetivas quanto maior for a atividade inflamatória e quanto mais precoce a fase da doença. Por isso, pacientes com EM altamente ativa requerem um tratamento de alta eficácia precocemente no curso da sua doença.7
A transição entre terapias pode ser um período de vulnerabilidade
Nas transições entre terapias, as medicações podem ser sequenciadas com intervalo insuficiente, resultando em efeitos nocivos, ou excessivo, expondo o paciente a uma latência terapêutica com possibilidade de surtos, atividade na RMN e/ou aumento da incapacidade. A escolha de medicações mais eficazes requer transições menos frequentes para outras terapias e, consequentemente, uma menor exposição dos pacientes a esses possíveis riscos.1 Como a eficiência dos métodos atualmente disponíveis de monitoramento da EM, por meio de medidas clínicas e radiológicas, é no máximo razoável, o neurologista que procura sinais evidentes de falha do tratamento para se decidir pelo escalonamento pode ser mal aconselhado.1
O conceito de reserva neurológica
Em indivíduos saudáveis, a atrofia cerebral por perda neuronal começa após os 20 anos de idade, mas a função neurológica pode manter-se normal até o fim da vida graças a uma “reserva cerebral e cognitiva”. Em estudos sobre a demência, os termos “reserva cerebral” e “reserva cognitiva” foram propostos como conceitos para ajudar a explicar a capacidade do cérebro de compensar as lesões sofridas, ao menos na fase inicial da doença.8
O máximo volume cerebral atingido ao longo da vida conteria uma “reserva cerebral” capaz de proteger contra o declínio cognitivo, que só se tornaria aparente após um comprometimento além de determinado limite. De maneira similar, o enriquecimento intelectual e as atividades e comportamentos que mantêm o cérebro ativo também constituiria uma “reserva cognitiva” protetora contra o declínio cognitivo.8
Já se demonstrou que esses conceitos se estendem à EM, e o termo “reserva neurológica” foi proposto para incluir outras funções neurológicas afetadas na EM, como as funções motora e sensorial. A teoria oferece respaldo científico para a intervenção precoce com TAE, ajudando os pacientes com EM a adotar um estilo de vida ativo e sadio que lhes permita construir uma reserva neurológica e melhorar suas funções neurológicas ao longo da evolução da doença.8
Clique aqui e descubra como Biogen Linc pode transformar sua rotina clínica.
Autoria

Felipe Resende Nobrega
Residência Médica em Neurologia (UNIRIO) • Mestre em Neurologia (UNIRIO) • Professor de Clínica Médica da UNESA
Como você avalia este conteúdo?
Sua opinião ajudará outros médicos a encontrar conteúdos mais relevantes.

