A maioria dos pacientes com formas recorrentes da esclerose múltipla (EM) necessitará de mais de uma droga modificadora do curso da doença (DMD) ao longo do seu tratamento para controlar a doença e limitar o agravamento da sua incapacidade. Ao sequenciar terapias, é importante reconhecer que determinada terapia pode afetar as escolhas terapêuticas futuras. Antes de iniciar o tratamento, o clínico deve desenvolver um plano de sequenciamento para que preocupações com a segurança ou outros fatores não limitem as opções terapêuticas subsequentes ou retardem o início da próxima DMD.1
Impacto imunológico das terapias com DMDs e implicações no tratamento
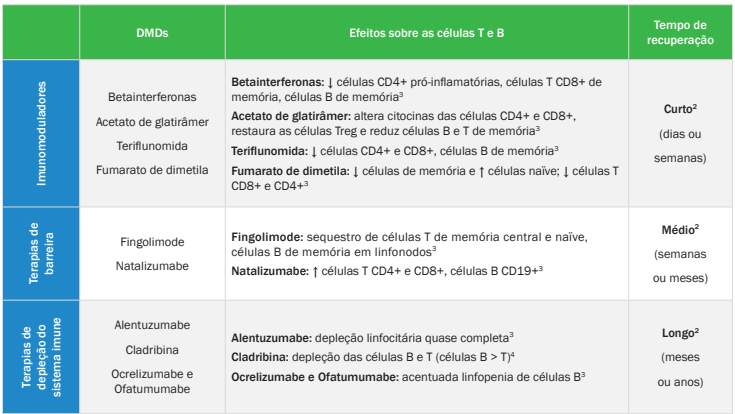
Todas as DMDs supostamente atenuam processos inflamatórios imunologicamente mediados no sistema nervoso central, levando à melhora em desfechos clínicos e radiológicos. Entretanto, algumas DMDs estão associadas a efeitos duradouros no sistema imunológico e/ou a eventos adversos graves, dois fatores que podem complicar o uso de terapias subsequentes.2 (Quadro 1)
Quadro 1. Efeitos das classes de DMDs sobre as populações de células B e T de pacientes com EM
Diferentes períodos de washout para troca entre DMSs
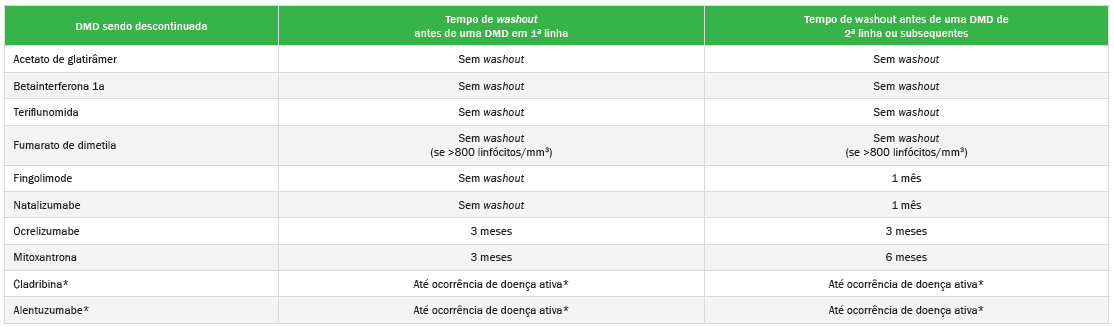
Outro fator que influencia as opções terapêuticas futuras na sequência do tratamento da EM é o intervalo sem medicação (washout) requerido pela DMD antes de sua introdução. A Sociedade Francesa de EM propõe os seguintes períodos de washout para troca entre as DMDs, visando prevenir eventos adversos por efeitos cumulativos.5 (Tabela 1)
Tabela 1. Períodos de washout recomendados para a transição entre terapias com diferentes DMDs
Eficácia e segurança de trocas entre diferentes DMDs
Mecanismos de ação distintos determinam diferenças nas transições entre as DMDs, em termos de repercussões imunológicas e riscos associados, no tratamento de pacientes com EM recorrente-remitente (EMRR). A tabela 2 ilustra algumas dessas diferenças.6-12
Tabela 2. Repercussões imunológicas da transição de terapia com natalizumabe para outras DMDs e de outras DMDs para natalizumabe

Terapias de reconstituição imunológica (TRI), como a cladribina e o alentuzumabe, exercem efeitos imunossupressores prolongados.12 Como a duração real dos efeitos dos imunossupressores da TRI é desconhecida,12 a transição para natalizumabe em pacientes JCV+ requer uma avaliação cuidadosa.7 Embora não existam estudos que comprovem um risco aumentado de LEMP nesse contexto, é importante considerar o impacto imunológicos das terapias prévias ao definir a melhor estratégia de tratamento.7
Taxas de eventos adversos associados a diferentes DMDs: dados de metanálise
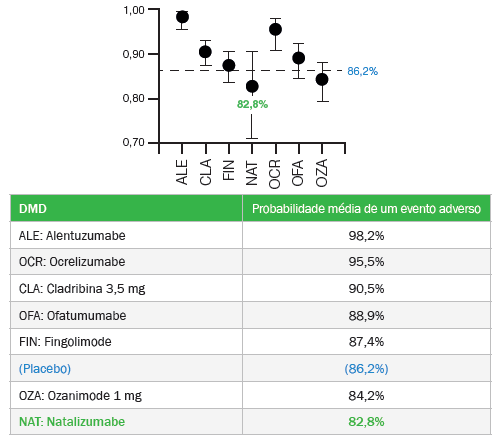
Em uma revisão sistemática e metanálise em rede que comparou a segurança de várias DMDs no tratamento da EM, o natalizumabe apresentou a mais baixa probabilidade de um evento adverso de qualquer grau entre todas as DMDs avaliadas, (Figura 1) inclusive em comparação com o placebo.13
Figura 1. Probabilidade média de evento adverso entre as DMDs incluídas na metanálise
Resultados de longo prazo do tratamento com natalizumabe
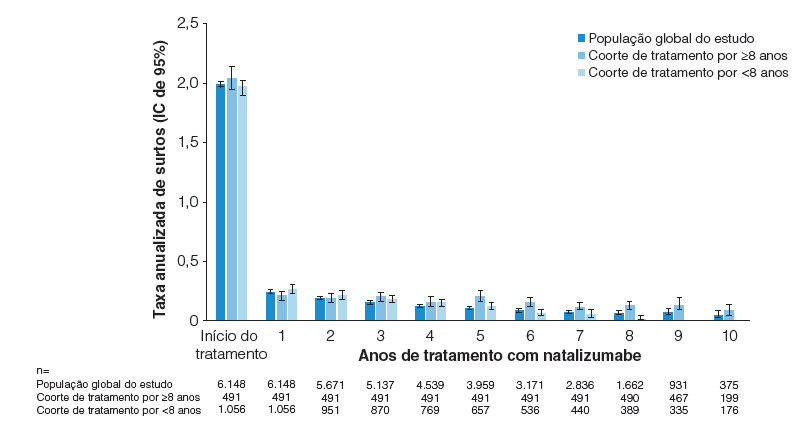
A figura 2 mostra as taxas anualizadas de surtos da doença em 6.148 pacientes com EMRR tratados com natalizumabe, no ano prévio ao início do tratamento e ao longo de dez anos de observação, de acordo com dados do registro TOP (programa de observação dos pacientes tratados com natalizumabe, do original Tysabri Observational Program). Durante o acompanhamento por dez anos, a taxa anualizada de surtos da EMRR foi de 0,15 (intervalo de confiança [IC] de 95%: 0,14 a 0,15), o que representa uma redução de 92,5% em relação à taxa observada no ano prévio ao início do tratamento, de 1,99 (IC de 95%: 1,97 a 2,02).14
Figura 2. Taxas anualizadas de surtos da EMRR em pacientes tratados com natalizumabe, na população global do registro TOP, nos pacientes que haviam sido tratados com natalizumabe por 8 anos ou mais e nos pacientes que haviam sido incluídos no programa mais de 8 anos antes da data de corte, mas que descontinuaram o tratamento com natalizumabe antes de completarem 8 anos de tratamento. As taxas basais referem-se ao período de um ano prévio ao início do tratamento com natalizumabe. As barras de erro indicam os intervalos de confiança de 95%.
Planejamento familiar na EM – entre as Terapias de Alta Eficácia aprovadas para uso no Brasil, somente natalizumabe não demanda contracepção durante o tratamento.7,15
O planejamento familiar é um fator essencial a ser considerado no sequenciamento terapêutico da esclerose múltipla (EM). Algumas terapias são contraindicadas ou não recomendadas durante a gestação, enquanto outras exigem o uso de contracepção ao longo do tratamento e por um período específico após a última dose.7,15-18 (Tabelas 3 e 4)
Tabela 3. Recomendações para o uso de DMDs durante a gravidez e a amamentação
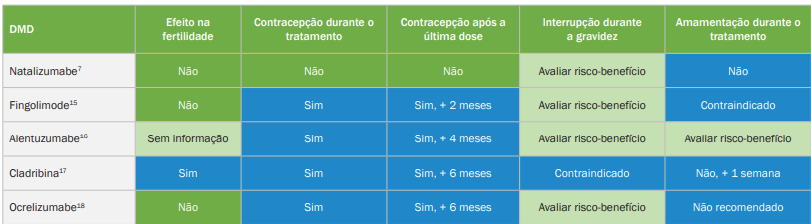
Tabela 4. Recomendações para o uso de DMDs durante o planejamento familiar

Natalizumabe: Terapia de Alta Eficácia indicada na 1ª linha do manejo da EM
Tanto no sistema público de saúde quanto no privado, natalizumabe é indicado como primeira linha de alta eficácia para o tratamento da EM.
- Sistema público: No Protocolo Clínico e Diretrizes Terapêuticas (PCDT), do Sistema Único de Saúde (SUS), natalizumabe é indicado:
Para pacientes virgens de tratamento ou não com alta atividade da doença ou na terceira linha para pacientes com baixa a moderada atividade da doença, após falha ou contraindicação de terapias prévias.19
- Sistema privado: Nas Diretrizes de Utilização (DUT) da Agência Nacional de Saúde Suplementar (ANS), natalizumabe é indicado:
Para pacientes virgens de tratamento com doença grave em rápida evolução ou nas terceira e quarta linhas, após falha ou contraindicação de terapias prévias.20
Em uma revisão sistemática e metanálise em rede que comparou a segurança de várias DMDs no tratamento da EM, o natalizumabe apresentou a mais baixa probabilidade de um evento adverso de qualquer grau entre todas as DMDs avaliadas, inclusive em comparação com o placebo.13
Durante o acompanhamento por dez anos, a taxa anualizada de surtos da EMRR foi de 0,15 (intervalo de confiança [IC] de 95%: 0,14 a 0,15), o que representa uma redução de 92,5% em relação à taxa observada no ano prévio ao início do tratamento, de 1,99 (IC de 95%: 1,97 a 2,02).14
Em suma, todos os pacientes com diagnóstico de esclerose múltipla recorrente-remitente (EMRR) clinicamente definida devem receber droga modificadora da doença (DMD). Há evidências consideráveis de que o tratamento precoce é benéfico e hoje temos um amplo arsenal terapêutico disponível.19 A escolha da melhor opção e do planejamento terapêutico requer avaliação cuidadosa que pondere individualmente o perfil de cada paciente, considerando fatores demográficos, clínicos e radiológicos, assim como os valores e preferências dos pacientes numa decisão compartilhada.20
Um dos possíveis fatores que podem influenciar no planejamento terapêutico é a disponibilidade da medicação, que pode ser limitada, devido ao custo e restrições de planos de saúde. No âmbito do SUS, o PCDT da EM propõe um algoritmo para uso das DMDs em pacientes com EM de baixa/moderada ou alta atividade21 e há pré-requisitos para obter os mesmos pela rede privada de saúde.22
Clique aqui e descubra como Biogen Linc pode transformar sua rotina clínica.
Autoria

Felipe Resende Nobrega
Residência Médica em Neurologia (UNIRIO) • Mestre em Neurologia (UNIRIO) • Professor de Clínica Médica da UNESA
Como você avalia este conteúdo?
Sua opinião ajudará outros médicos a encontrar conteúdos mais relevantes.

