A esclerose múltipla (EM) é uma doença desmielinizante do Sistema Nervoso Central (SNC) e atinge principalmente adultos jovens, com potencial de deixar acometimentos funcionais que interferem nas atividades da vida diária. É de suma importância o tratamento precoce com drogas modificadoras do curso da doença (DMDs), tendo em vista que estudos observacionais sugerem que seu uso está associado a um menor risco a longo prazo de progressão da doença, ou seja, um impacto importante na qualidade de vida dos pacientes.1 Os principais objetivos do tratamento com DMDs são prevenir recidivas (surtos) e reduzir o acúmulo de incapacidades neurológicas ao longo do tempo.1
Uma série de fatores, como demográficos, clínicos e radiológicos, podem ajudar a orientar as opções de DMDs. Os médicos devem avaliar os pacientes na apresentação e periodicamente a partir de então quanto a características associadas a um mau prognóstico e maior risco de recidiva futura e incapacidade grave. Os fatores mais importantes que predizem uma pior evolução clínica e resultados desfavoráveis a longo prazo são a presença de doença altamente ativa (por exemplo, recidivas frequentes e novas lesões de ressonância magnética), extenso envolvimento radiológico, lesões na medula espinhal e/ou recuperação incompleta das recidivas. Pacientes com essas características podem ser bons candidatos para iniciar o tratamento com Terapia de Alta Eficácia (TAE), como o natalizumabe.1
O natalizumabe é um anticorpo monoclonal recombinante humanizado anti-integrina α-4, indicado como terapia única no tratamento da esclerose múltipla recorrente-remitente (EMRR), para prevenir e retardar a progressão da incapacidade em pacientes que não responderam a um ciclo completo e adequado de outros medicamentos, ou com EMRR grave em rápida evolução.2
Melhores desfechos clínicos com a troca para natalizumabe
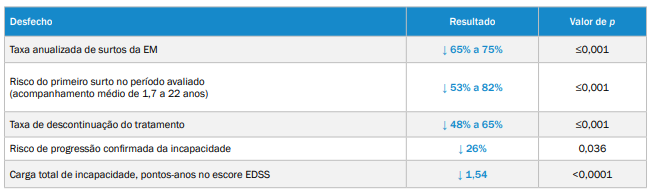
Em pacientes com esclerose múltipla (EM) que apresentaram surto da doença durante a terapia inicial com betainterferona (IFN-β) ou acetato de glatirâmer (AG), a troca para natalizumabe levou a melhores desfechos clínicos, em comparação com a troca para AG ou IFN-β:3
Tabela 1. Desfechos clínicos observados em pacientes com EM que trocaram para natalizumabe, comparados a pacientes que trocaram para AG ou IFN-β
Menor probabilidade cumulativa de surtos com natalizumabe vs. fingolimode
O estudo prospectivo e randomizado de fase 4 REVEAL comparou a eficácia de natalizumabe e fingolimode em 108 pacientes com EMRR de nove países. Em 36 semanas, a probabilidade cumulativa de surto da doença foi de 1,9% com natalizumabe e 22,3% com fingolimode:4
Figura 1. Curvas de sobrevida de Kaplan-Meier do tempo até um surto da EM ao longo de 52 semanas
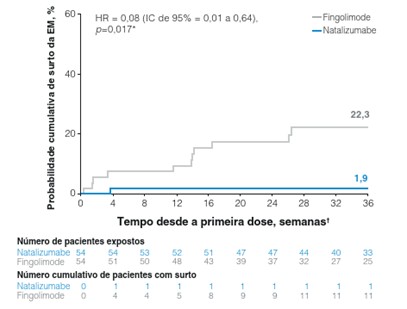
EM: esclerose múltipla; EDSS: Escala Expandida do Estado de Incapacidade (Expanded Disability Status Scale); HR: razão de risco (hazard ratio).
Adaptada de: Butzkueven H, et al. BMJ Open. 2020 Oct 20;10(10):e038861.4
Novas lesões Gd+ na RMN com natalizumabe vs. fingolimode
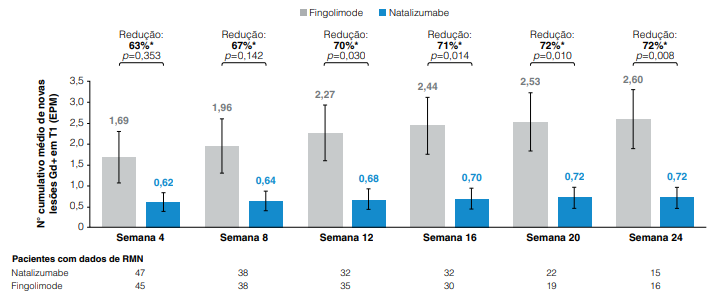
No mesmo estudo REVEAL, o número cumulativo médio de novas lesões realçadas por gadolínio nas imagens de RMN ponderadas em T1 em 24 semanas foi de 0,72 com natalizumabe e 2,60 com fingolimode.4
Figura 2. Número cumulativo médio de novas lesões Gd+ em imagens de RMN ponderadas em T1 ao longo de 24 semanas do estudo REVEAL
Menor taxa de surtos anualizada com natalizumabe vs. cladribina
Dados do estudo de fase 3 CLARITY que avaliaram a cladribina em comprimidos vs. placebo foram pareados por escores de propensão aos dados do registro italiano i-MuST de 3.150 pacientes com EMRR que iniciaram uma DMD. A análise comparou a taxa anualizada de surtos da doença em 2 anos após o início do tratamento com cladribina (n=945) vs. outras DMDs – IFN (n=1.168), AG (n=402), FING (n = 113), NTZ (n=149) e DMF (n=295) –, tomando-se as comparações com placebo como referência. O efeito terapêutico foi estimado por meio de um modelo de regressão binomial negativo com ponderação por probabilidade inversa. Uma análise de sensibilidade que incluiu a atividade basal ao exame de RMN no cálculo dos escores de propensão foi realizada no subgrupo de pacientes com dados basais de RMN disponíveis.5
Figura 3. Taxas anualizadas de surtos da EM em pacientes tratados com cladribina vs. outras DMDs
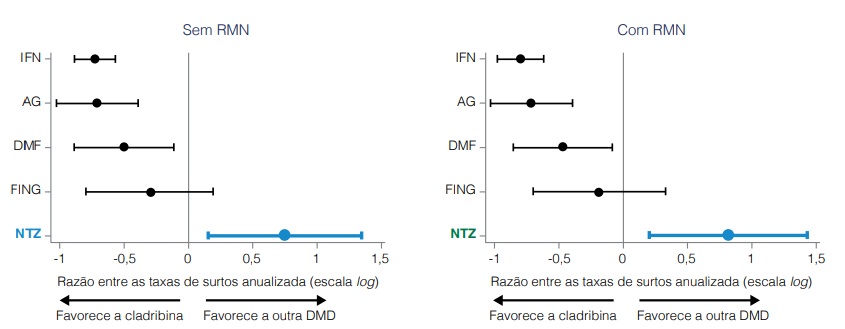
Na análise, natalizumabe foi superior à cladribina, com razão entre as taxas anualizadas de surtos da EM de 2,13 (p=0,014). A razão das taxas de natalizumabe vs. placebo foi de 82% (gráfico da esquerda). Resultados similares foram obtidos na análise do subgrupo que incluiu a atividade basal da doença no exame de RMN no cálculo dos escores de propensão (gráfico da direita).
Menor taxa de eventos adversos entre as DMDs
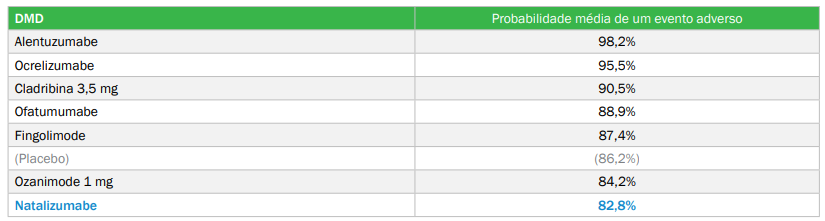
Em uma revisão sistemática e metanálise em rede que comparou a segurança de várias drogas modificadoras do curso da doença (DMDs) no tratamento da EM, o natalizumabe exibiu a mais baixa probabilidade de um evento adverso de qualquer grau entre todas as DMDs avaliadas, (Tabela 2) inclusive em comparação com o placebo.6
Tabela 2. Probabilidade média de evento adverso entre as DMDs incluídas na metanálise
Comparação indireta entre natalizumabe e ocrelizumabe
Uma comparação indireta pareada por escores de propensão com dados do Registro Italiano de Esclerose Múltipla avaliou os efeitos de natalizumabe e ocrelizumabe sobre a progressão independente de surtos da doença (desfecho PIRA, do original progression independent of relapse activity), piora associada a surto da doença e escores 4,0 e 6,0 na Escala Expandida do Estado de Incapacidade (EDSS, do original Expanded Disability Status Scale) em pacientes com EM virgens de tratamento.7
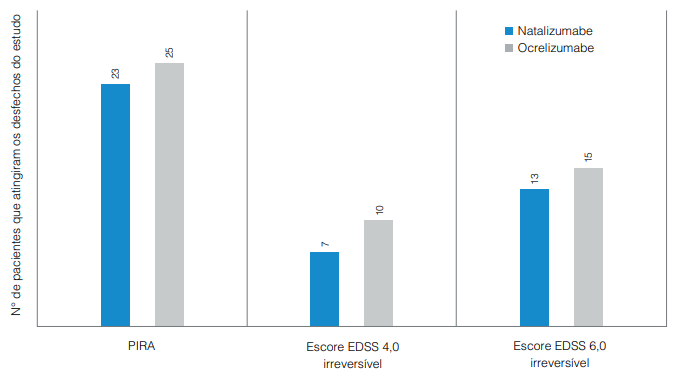
- No curto prazo, o risco de atingir os eventos PIRA e escores EDSS 4,0 e 6,0 irreversíveis não foi significativamente diferente entre as duas medicações.
Figura 4. Número de pacientes que atingiram os eventos PIRA e escores EDSS 4,0 e 6,0 irreversíveis nas coortes pareadas por escore de propensão tratadas com natalizumabe e ocrelizumabe do Registro Italiano de Esclerose Múltipla.
Qualidade de vida com natalizumabe vs. ocrelizumabe
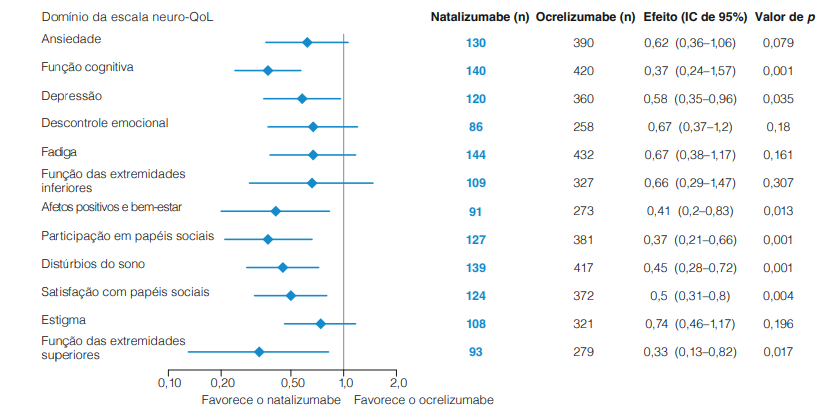
Uma análise de dados da rede MS PATHS avaliou o tempo até a melhora na escala de qualidade de vida em transtornos neurológicos Neuro-QoL em pacientes tratados com natalizumabe ou ocrelizumabe. Observou-se melhora significativa em 9 e 4 dos 12 domínios da escala Neuro-QoL com natalizumabe vs. ocrelizumabe, respectivamente. Em sete domínios da escala Neuro-Qol, a melhora clinicamente significativa foi mais rápida com natalizumabe, comparado ao ocrelizumabe: função cognitiva, depressão, afetos positivos e bem-estar, participação em papéis sociais, distúrbios do sono, função das extremidades superiores e satisfação com papéis sociais.7
Figura 5. Tempo até a melhora em domínios da escala Neuro-QoL em pacientes com EM tratados com natalizumabe vs. ocrelizumabe
Metanálise da taxa anualizada de surtos da EM
Em revisão sistemática e metanálise em rede de 40 estudos clínicos randomizados e controlados, envolvendo ao todo 28.391 participantes, 20 tratamentos mais o placebo, todas as terapias, exceto a β-interferona 1a 22 μg por via subcutânea, foram estatisticamente superiores ao placebo em termos de taxa anualizada de surtos da EM.9
Na análise, natalizumabe foi superior ao placebo com razão de risco (RR) de 0,31 (IC de 95%: 0,27 a 0,37) e não foi significativamente inferior a nenhuma das outras DMDs, com diferenças significativas em favor do natalizumabe nas comparações com ozanimode, fingolimode, fumarato de dimetila, ponesimode, todas as β-interferonas avaliadas, acetato de glatirâmer e teriflunomida.9
Figura 6. Taxa anualizada de surtos da EM em pacientes tratados com 20 DMDs diferentes, comparadas entre si e em relação ao placebo

Apesar do custo elevado das DMDs, existem formas de os pacientes obterem acesso e iniciarem o tratamento, desde que preencham os pré-requisitos estabelecidos para o seu uso, seja no sistema de Saúde Único de Saúde (SUS), seja no privado. No entanto, é importante reforçar que nem todos os tratamentos são cobertos por esses sistemas, sendo necessário compreender as especificidades de cada um.10, 11
Destaca-se, ainda, que toda tomada de decisão médica relacionada ao início de DMDs deve ser compartilhada com o paciente, sendo preciso levar em consideração seus valores e preferências, o colocando no centro dos cuidados.12
Clique aqui e descubra como Biogen Linc pode transformar sua rotina clínica.
Autoria

Felipe Resende Nobrega
Residência Médica em Neurologia (UNIRIO) • Mestre em Neurologia (UNIRIO) • Professor de Clínica Médica da UNESA
Como você avalia este conteúdo?
Sua opinião ajudará outros médicos a encontrar conteúdos mais relevantes.

